Investigación
Descifran cómo humanos y levaduras deciden si crecer o no según haya alimento

El texto se ha copiado correctamente en el portapapeles
Un equipo del Centro Nacional de Investigaciones Oncológicas (CNIO) informó este viernes de nuevos hallazgos en el estudio de TOR, la "gran proteína que permite a las células detectar si hay nutrientes disponibles y decidir si deben crecer o frenar su actividad", un mecanismo clave en el desarrollo de enfermedades como el cáncer y en el diseño de nuevos tratamientos más precisos.
El hallazgo, publicado en la revista 'Nature Structural & Molecular Biology', resuelve la estructura de uno de los interruptores moleculares que regulan esta proteína, TOR, presente en multitud de especies, desde levaduras y plantas hasta animales y seres humanos, y considerada "uno de los engranajes centrales del crecimiento celular".
El investigador del CNIO Lucas Tafur describió cómo funciona uno de los complejos que controlan la actividad de TOR, una proteína que actúa como un sistema de decisión biológica común a muchos seres vivos. “Todas las células tienen mecanismos para percibir cuántos nutrientes hay y transmitir esa información a las proteínas que regulan el crecimiento celular”, explicó Tafur. “Cuando faltan nutrientes, TOR se inhibe y la célula frena el crecimiento, y cuando hay recursos suficientes, como aminoácidos o glucosa, TOR se activa y promueve la proliferación”.
Comprender con detalle este proceso es fundamental porque el mal funcionamiento de TOR está relacionado con enfermedades como el cáncer, trastornos metabólicos o alteraciones del desarrollo.
Según el investigador, intervenir directamente sobre esta proteína puede provocar efectos secundarios importantes, por lo que conocer con precisión cómo se regula abre nuevas vías terapéuticas. “Si entendemos en detalle la maquinaria que regula a TOR, podemos encontrar la manera de intervenir de forma más selectiva”, señaló.
LA RAPAMICINA DE LA ISLA DE PASCUA
Acrónimo de 'Target of Rapamycin', TOR debe su nombre a la rapamicina, un compuesto descubierto en la década de 1970 en muestras recogidas en la Isla de Pascua en los años 64 y 65 del pasado siglo y que hoy se utiliza en fármacos inmunosupresores y anticancerígenos. Décadas después se comprobó que esta molécula actúa precisamente sobre TOR, lo que convirtió a esta proteína "en uno de los grandes objetivos de la investigación biomédica", según el CNIO.
El origen del hallazgo se remonta a la llamada Expedición Médica a la Isla de Pascua (Metei), organizada en 1964 por el cirujano Stanley Skoryna y el bacteriólogo Georges Nogrady. Con financiación de la Organización Mundial de la Salud (OMS) y apoyo logístico de la Marina canadiense, pretendían estudiar cómo una población aislada respondía a los cambios ambientales derivados de la construcción de un aeropuerto internacional.
Una de los centenares de muestras recolectadas en el suelo por los científicos contenía la bacteria 'Streptomyces hydroscopicus', a la postre productora de la molécula de la rapamicina. Tras su llegada a Canadá, las muestras fueron estudiadas en los laboratorios Ayerst, donde el investigador Suren Sehgal consiguió aislar la rapamicina y mantener viva la investigación pese a los recortes, conservando cultivos para evitar su desaparición, según fuentes históricas de la farmacología moderna. Años más tarde, el compuesto se comercializó como 'Rapamune', un hito en la farmacología moderna que abrió una nueva línea de tratamientos para el sistema inmunitario.
La rapamicina tiene propiedades inmunosupresoras y anticancerígenas y ya se usaba en varios fármacos (por ejemplo, para evitar el rechazo de trasplantes) antes de que en los años 90 se descubriera, usando levadura, que TOR es su diana. Es muy importante en biomedicina porque permite frenar el crecimiento celular, por eso se utiliza en trasplantes, cáncer e investigación sobre envejecimiento.
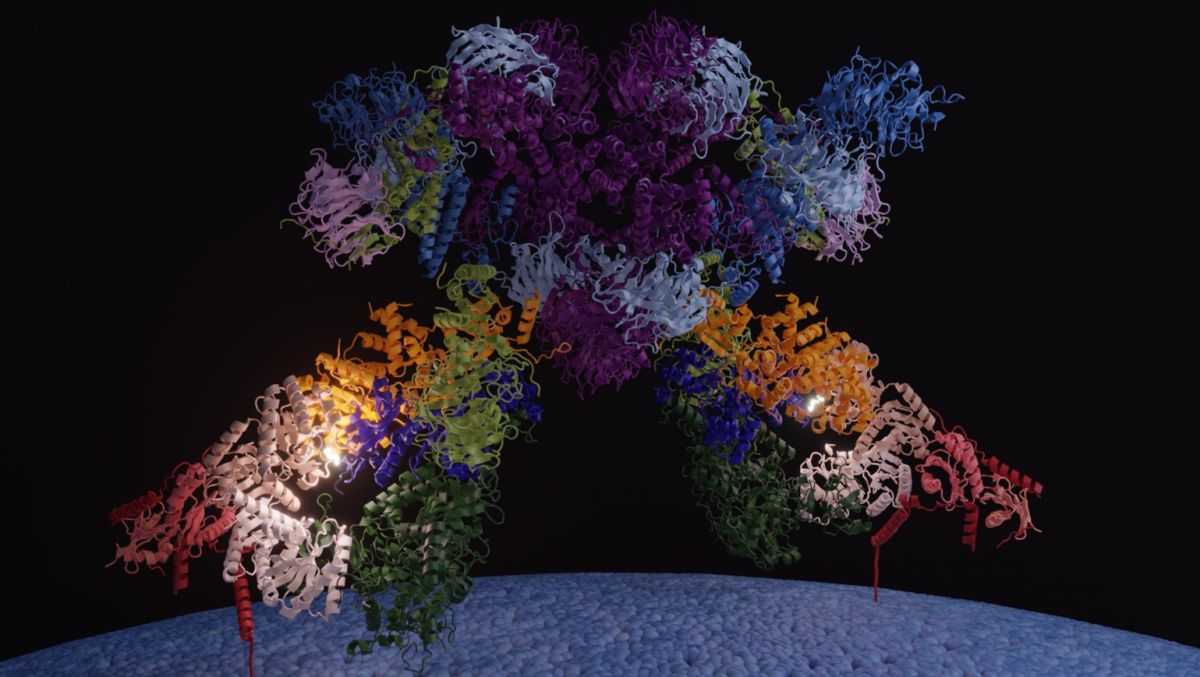
Esta proteína no actúa sola, sino formando grandes complejos moleculares que integran señales relacionadas con la presencia de nutrientes. En este trabajo, el equipo del CNIO resolvió la estructura del complejo SEA (también llamado Gator), un regulador clave que integra señales procedentes de aminoácidos, glucosa o colesterol y determina si TOR debe activarse o inhibirse.
INTERRUPTOR DE LA ACTIVIDAD CELULAR
El estudio del CNIO demostró que este sistema funciona de forma más coordinada de lo que se pensaba y que basta una pequeña alteración en uno de sus componentes para cambiar completamente la respuesta de la célula. “Es como un interruptor”, explicó Tafur. “No solo sirve para frenar la actividad de TOR, sino también para activarla rápidamente cuando hay nutrientes disponibles”.
El descubrimiento se realizó mediante crio-microscopía electrónica, una técnica que permite obtener imágenes tridimensionales de las proteínas a resolución casi atómica y que "está permitiendo reconstruir pieza a pieza el complejo mecanismo que controla el crecimiento celular".
Los investigadores destacaron que TOR se ha conservado a lo largo de miles de millones de años de evolución porque resuelve un problema común a todos los organismos: "saber si hay recursos suficientes para crecer o si es necesario ahorrar energía". Por eso, estudiar este sistema en levaduras "permite entender cómo funciona también en humanos, lo que convierte a este microorganismo en una herramienta clave para la investigación biomédica".
El CNIO subrayó que avances como este "ayudan a comprender mejor los procesos básicos de la vida y pueden facilitar el desarrollo de terapias más eficaces y menos tóxicas en el futuro", al permitir actuar con mayor precisión sobre los mecanismos que controlan el crecimiento de las células.
(SERVIMEDIA)
20 Mar 2026
EDU/gja