Investigación
Identifican un nuevo efecto del uso de nanopartículas de hierro en el crecimiento de células tumorales
El texto se ha copiado correctamente en el portapapeles
Un equipo del Consejo Superior de Investigaciones Científicas (CSIC) constató el potencial de distintos recubrimientos de nanopartículas de hierro como terapias inductoras de estrés oxidativo para tratar el cáncer, lo que abre nuevas vías para tratamientos antitumorales.
Un nuevo trabajo de investigadores del CSIC publicado en la revista 'Biomaterials' identifica recubrimientos de nanopartículas de óxido que afectan específicamente al crecimiento de las células tumorales al generar elevados niveles de estrés oxidativo que terminan afectando su metabolismo mitocondrial, lo que abre la posibilidad de su uso combinado en terapias ya establecidas.
Las nanopartículas de óxido de hierro son una novedosa herramienta en biomedicina, según el Consejo. "Su pequeño tamaño y la capacidad de nuestro cuerpo para metabolizarlas con muy baja toxicidad hace que sean adecuadas en métodos poco invasivos para el diagnóstico y el tratamiento de enfermedades como el cáncer, donde ya se habían usado para el transporte selectivo de fármacos".
Domingo F. Barber, investigador del CSIC en el Centro Nacional de Biotecnología (CNB-CSIC), director de la investigación, destacó que ahora se ha visto "que las propias nanopartículas y las moléculas de las que se recubren para su uso biomédico pueden tener efectos antitumorales; estas nanopartículas son como ‘nanocanicas sólidas’”.
Añadió que tienen un núcleo compacto de óxido de hierro que hay recubrir con diferentes materiales para proporcionar así más estabilidad y menos toxicidad. "Nuestro grupo lleva años analizando diferentes tipos de recubrimiento y viendo cómo afectan a su entrada en la célula, su acumulación y degradación dentro de la misma, pero hasta ahora no habíamos estudiado su efecto en el metabolismo celular a nivel global”.
El investigador apuntó que se sabía que las nanopartículas pueden aumentar el estrés oxidativo celular sin afectar de manera considerable al equilibrio a determinadas dosis. "Ahora nos preguntamos si algún tipo de recubrimiento podría potenciar aún más el estrés en células tumorales, donde la homeóstasis ya está desregulada, hasta niveles que conlleven la muerte celular de manera selectiva.”
Neus Daviu, también investigadora del CNB-CSIC, detalló el análisis realizado: “Hemos utilizado tres tipos de recubrimientos diferentes en las nanopartículas y probado si afectan al metabolismo celular tanto en líneas celulares modelo de diferentes tipos de tumor (mama, páncreas y glioma) como en líneas no tumorales de macrófagos y células endoteliales que también se pueden encontrar en los tumores”.
TRATAMIENTO
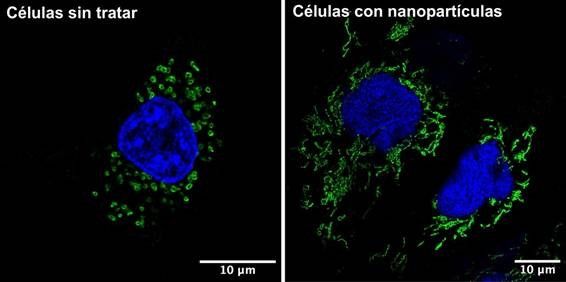
Los parámetros estudiados por los expertos son varios. Por un lado, la actividad metabólica de la célula, analizando el funcionamiento de las mitocondrias, el orgánulo encargado de la respiración. No sólo cambian su forma, un síntoma claro de mal funcionamiento, sino que producen menos ATP (la molécula esencial para producir energía) y se degradan más, ya que la célula detecta que funciona mal y las elimina en un proceso llamado autofagia.
Además, como señaló Daviu, “se produce una parada en el ciclo celular: las células tumorales tratadas con las nanopartículas cubiertas con DMSA (ácido dimercaptosucinico) crecen mucho menos, se quedan como ‘atascadas/atoradas’, un efecto muy deseado para frenar la proliferación de los tumores.”
Los investigadores destacaron el "efecto diferencial" en los distintos tipos celulares de tumor utilizados, "siendo los más sensibles al efecto de estas nanopartículas los de origen mamario". Aunque estos datos se han obtenido en líneas celulares, otros trabajos de los mismos autores apuntan a un mejor funcionamiento 'in vivo' (en ratones) de la terapia antitumoral cuando se administra a través de nanopartículas recubiertas con DMSA, "lo que remarca su potencial para el transporte dirigido de fármacos y su colaboración en la reducción de los tumores", remachó el CSIC.
(SERVIMEDIA)
10 Ene 2024
CAG/gja



